ทฤษฎีปรมาณูมาไกลกว่าไม่กี่พันปีที่ผ่านมา เริ่มขึ้นในช่วงคริสตศักราชศตวรรษที่ 5 ด้วยทฤษฎีเดโมแครเชียลเรื่อง "คอร์คัส" ที่มีปฏิสัมพันธ์ซึ่งกันและกันโดยกลไกจากนั้นก็เคลื่อนไปสู่โมเดลอะตอมของดาลตันในศตวรรษที่ 18 จากนั้นจะครบกำหนดในศตวรรษที่ 20 ด้วยการค้นพบอนุภาคอะตอม การเดินทางของการค้นพบนั้นยาวนานและคดเคี้ยว
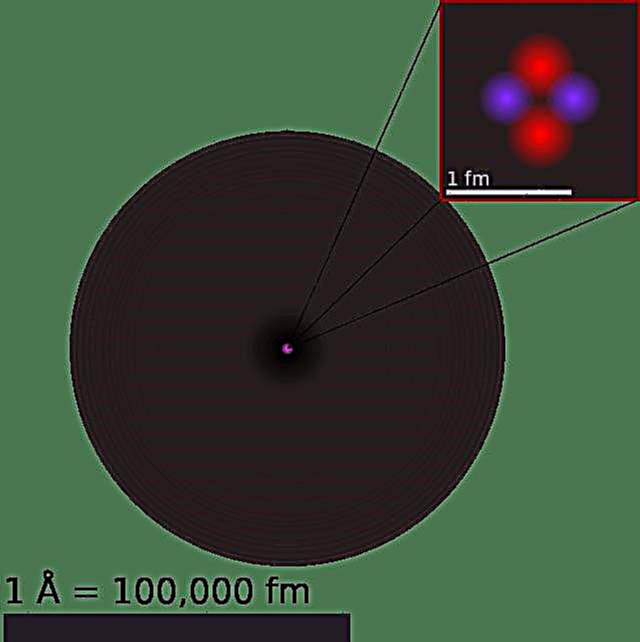
อาจเป็นหนึ่งในเหตุการณ์สำคัญที่สำคัญที่สุดระหว่างทางเป็นแบบจำลองอะตอมของ Bohr ซึ่งบางครั้งเรียกว่าแบบจำลองอะตอมของ Rutherford-Bohr นำเสนอโดย Niels Bohr นักฟิสิกส์ชาวเดนมาร์กในปี 1913 รุ่นนี้แสดงให้เห็นว่าอะตอมเป็นนิวเคลียสที่มีประจุบวกเล็ก ๆ ล้อมรอบด้วยอิเล็กตรอนที่เคลื่อนที่เป็นวงกลม (กำหนดตามระดับพลังงาน) รอบศูนย์กลาง
ทฤษฎีปรมาณูสู่ศตวรรษที่ 19:
ตัวอย่างที่รู้จักกันเร็วที่สุดของทฤษฎีปรมาณูมาจากกรีกโบราณและอินเดียซึ่งนักปรัชญาเช่น Democritus ได้รับการกล่าวอ้างว่าสสารทั้งหมดประกอบด้วยหน่วยเล็ก ๆ แบ่งแยกไม่ได้และทำลายไม่ได้ คำว่า "อะตอม" ถูกประกาศเกียรติคุณในกรีซโบราณและก่อให้เกิดโรงเรียนแห่งความคิดที่เรียกว่า "อะตอม" อย่างไรก็ตามทฤษฎีนี้เป็นแนวคิดทางปรัชญามากกว่าแนวคิดทางวิทยาศาสตร์
จนกระทั่งศตวรรษที่ 19 ทฤษฎีของอะตอมได้กลายเป็นเสียงก้องเป็นเรื่องทางวิทยาศาสตร์โดยมีการทดลองตามหลักฐานครั้งแรก ตัวอย่างเช่นในช่วงต้นปี 1800 นักวิทยาศาสตร์ชาวอังกฤษ John Dalton ใช้แนวคิดของอะตอมเพื่ออธิบายว่าทำไมองค์ประกอบทางเคมีจึงมีปฏิกิริยาในรูปแบบที่สามารถสังเกตเห็นได้ จากการทดลองเกี่ยวกับก๊าซหลายครั้งดัลตันก็ทำการพัฒนาสิ่งที่เรียกว่าทฤษฎีอะตอมของดัลตัน
ทฤษฎีนี้ขยายตัวในกฎของการสนทนาของมวลและสัดส่วนที่แน่นอนและลงมาถึงสถานที่ห้า: องค์ประกอบในสภาพที่บริสุทธิ์ของพวกเขาประกอบด้วยอนุภาคที่เรียกว่าอะตอม; อะตอมขององค์ประกอบเฉพาะนั้นเหมือนกันหมดไปจนถึงอะตอมสุดท้าย อะตอมของธาตุต่าง ๆ สามารถบอกได้ด้วยน้ำหนักอะตอม อะตอมขององค์ประกอบรวมตัวกันเป็นสารประกอบทางเคมี อะตอมไม่สามารถสร้างหรือถูกทำลายในปฏิกิริยาทางเคมีมีเพียงการจัดกลุ่มเท่านั้นที่เปลี่ยนแปลง
การค้นพบอิเล็กตรอน:
ในปลายศตวรรษที่ 19 นักวิทยาศาสตร์เริ่มตั้งทฤษฎีว่าอะตอมประกอบด้วยหน่วยพื้นฐานมากกว่าหนึ่งหน่วย อย่างไรก็ตามนักวิทยาศาสตร์ส่วนใหญ่กล้าที่หน่วยนี้จะเป็นขนาดของอะตอมที่รู้จักกันน้อยที่สุด - ไฮโดรเจน ในตอนท้ายของศตวรรษที่ 19 สิ่งนี้จะเปลี่ยนไปอย่างมากขอบคุณการวิจัยที่จัดทำโดยนักวิทยาศาสตร์อย่างเซอร์โจเซฟจอห์นทอมสัน
จากการทดลองใช้หลอดรังสีแคโทด (รู้จักกันในชื่อ Crookes ’Tube) ทอมสันพบว่ารังสีแคโทดอาจเบี่ยงเบนไปจากสนามไฟฟ้าและสนามแม่เหล็ก เขาสรุปว่าแทนที่จะประกอบด้วยแสงพวกมันประกอบด้วยอนุภาคที่มีประจุลบซึ่งมีขนาดเล็กกว่า 1ooo 1 เท่าและเบากว่าไฮโดรเจน 1,800 เท่า

สิ่งนี้พิสูจน์หักล้างความคิดได้อย่างมีประสิทธิภาพว่าอะตอมไฮโดรเจนเป็นหน่วยที่เล็กที่สุดของสสารและ Thompson ก็ไปไกลกว่านี้เพื่อแนะนำว่าอะตอมนั้นสามารถแบ่งได้ เพื่ออธิบายค่าใช้จ่ายโดยรวมของอะตอมซึ่งประกอบด้วยประจุทั้งบวกและลบทอมป์สันเสนอแบบจำลองโดยที่ "corpuscles" ที่มีประจุลบถูกกระจายในทะเลที่มีประจุบวก - รู้จักกันในชื่อพลัมพุดดิ้ง
ศพเหล่านี้จะถูกเรียกว่า "อิเล็กตรอน" ในภายหลังตามทฤษฎีเชิงทฤษฎีที่นักฟิสิกส์แองโกล - ไอริชคาดการณ์ไว้จอร์จจอห์นสโตนสโตนนี่ในปี 1874 และจากนี้รูปแบบพลัมพุดดิ้งถือกำเนิดขึ้น เค้กลูกพลัมและลูกเกด แนวคิดได้รับการแนะนำให้รู้จักกับโลกในฉบับเดือนมีนาคม 1904 ของ นิตยสารเชิงปรัชญา เพื่อเสียงไชโยโห่ร้อง
รุ่นรัทเธอร์ฟอร์ด:
การทดลองครั้งต่อมาเผยปัญหาทางวิทยาศาสตร์จำนวนหนึ่งกับแบบจำลองพลัมพุดดิ้ง สำหรับผู้เริ่มมีปัญหาในการแสดงให้เห็นว่าอะตอมมีประจุพื้นหลังเป็นบวกซึ่งต่อมาถูกเรียกว่า "ปัญหาทอมสัน" ห้าปีต่อมาแบบจำลองจะถูกหักล้างโดย Hans Geiger และ Ernest Marsden ผู้ทำการทดลองหลายชุดโดยใช้อนุภาคแอลฟาและฟอยล์สีทอง - หรือที่รู้จักกันว่า “ การทดลองฟอยล์สีทอง”
ในการทดลองนี้ Geiger และ Marsden วัดรูปแบบการกระเจิงของอนุภาคแอลฟาด้วยหน้าจอเรืองแสง หากแบบจำลองของทอมสันถูกต้องอนุภาคแอลฟาจะผ่านโครงสร้างอะตอมของฟอยล์ที่ไม่มีข้อ จำกัด อย่างไรก็ตามพวกเขาตั้งข้อสังเกตว่าในขณะที่ยิงตรงส่วนใหญ่บางคนกระจัดกระจายไปในทิศทางต่าง ๆ กับบางคนกลับไปในทิศทางของแหล่งที่มา

Geiger และ Marsden สรุปว่าอนุภาคได้เผชิญกับแรงไฟฟ้าสถิตมากกว่าที่โมเดลของ Thomson อนุญาต เนื่องจากอนุภาคอัลฟาเป็นเพียงนิวเคลียสของฮีเลียม (ซึ่งมีประจุเป็นบวก) สิ่งนี้แสดงให้เห็นว่าประจุบวกในอะตอมไม่ได้แยกย้ายกันอย่างกว้างขวาง แต่กระจุกตัวในปริมาตรเล็กน้อย นอกจากนี้ความจริงที่ว่าอนุภาคเหล่านั้นที่ไม่ได้ถูกเบี่ยงเบนผ่านผ่านขัดขวางหมายความว่าพื้นที่เชิงบวกเหล่านี้ถูกแยกออกจากกันโดยอ่าวขนาดใหญ่ของพื้นที่ว่าง
ในปี 1911 Ernest Rutherford นักฟิสิกส์ได้ตีความการทดลองของ Geiger-Marsden และปฏิเสธแบบจำลองอะตอมของ Thomson แต่เขาเสนอแบบจำลองที่อะตอมประกอบด้วยพื้นที่ว่างส่วนใหญ่โดยประจุบวกทั้งหมดจะรวมอยู่ในจุดศูนย์กลางในปริมาตรเล็ก ๆ ที่ล้อมรอบด้วยกลุ่มอิเล็กตรอน เรื่องนี้เป็นที่รู้จักในนามรุทเธอร์เฟิร์ดโมเดลของอะตอม
รุ่น Bohr:
การทดสอบครั้งต่อไปโดย Antonius Van den Broek และ Niels Bohr ได้ทำการปรับปรุงแบบจำลองต่อไป ในขณะที่ Van den Broek แนะนำว่าหมายเลขอะตอมของธาตุนั้นคล้ายกับประจุนิวเคลียร์มาก ๆ แต่อะตอมหลังเสนอรูปแบบคล้ายกับระบบสุริยะของอะตอมโดยที่นิวเคลียสมีจำนวนประจุบวกและล้อมรอบด้วยค่าที่เท่ากัน จำนวนอิเล็กตรอนในเปลือกวงโคจร (aka. the Bohr Model)
นอกจากนี้แบบจำลองของ Bohr ได้ปรับปรุงองค์ประกอบบางอย่างของแบบจำลอง Rutherford ที่มีปัญหา สิ่งเหล่านี้รวมถึงปัญหาที่เกิดขึ้นจากกลไกคลาสสิกซึ่งคาดการณ์ว่าอิเล็กตรอนจะปล่อยคลื่นแม่เหล็กไฟฟ้าในขณะที่โคจรรอบนิวเคลียส เนื่องจากการสูญเสียพลังงานอิเล็กตรอนจะต้องวนเข้าด้านในอย่างรวดเร็วและยุบตัวเข้าไปในนิวเคลียส กล่าวโดยสรุปว่าแบบจำลองอะตอมนี้แสดงว่าอะตอมทั้งหมดไม่เสถียร

แบบจำลองยังทำนายอีกว่าเมื่ออิเล็กตรอนหมุนวนภายในการปล่อยของพวกมันจะเพิ่มความถี่อย่างรวดเร็วเมื่อวงโคจรเล็กลงและเร็วขึ้น อย่างไรก็ตามการทดลองกับการคายประจุไฟฟ้าในปลายศตวรรษที่ 19 พบว่าอะตอมปล่อยพลังงานแม่เหล็กไฟฟ้าที่ความถี่ไม่ต่อเนื่องบางตัวเท่านั้น
Bohr แก้ไขสิ่งนี้โดยเสนอว่าอิเล็กตรอนโคจรรอบนิวเคลียสด้วยวิธีที่สอดคล้องกับทฤษฎีควอนตัมของการแผ่รังสี ในรูปแบบนี้อิเล็กตรอนสามารถครอบครองวงโคจรที่ได้รับอนุญาตด้วยพลังงานบางอย่างเท่านั้น นอกจากนี้พวกเขาสามารถได้รับและสูญเสียพลังงานโดยการกระโดดจากวงโคจรที่อนุญาตไปยังอีกอันหนึ่งดูดซับหรือเปล่งรังสีแม่เหล็กไฟฟ้าในกระบวนการ
วงโคจรเหล่านี้เกี่ยวข้องกับพลังงานที่แน่นอนซึ่งเขาเรียกว่า เปลือกพลังงาน หรือ ระดับพลังงาน. กล่าวอีกนัยหนึ่งพลังงานของอิเล็กตรอนภายในอะตอมไม่ได้ต่อเนื่อง แต่เป็น "quantized" ระดับเหล่านี้จึงมีป้ายกำกับด้วยหมายเลขควอนตัม n (n = 1, 2, 3, ฯลฯ) ซึ่งเขาอ้างว่าสามารถตัดสินใจได้โดยใช้สูตร Ryberg ซึ่งเป็นกฎที่กำหนดขึ้นในปี 1888 โดยนักฟิสิกส์ชาวสวีเดนโยฮันเนส Ryberg เพื่ออธิบายความยาวคลื่นของเส้นสเปกตรัมขององค์ประกอบทางเคมีจำนวนมาก
อิทธิพลของรุ่น Bohr:
ในขณะที่แบบจำลองของ Bohr ได้พิสูจน์แล้วว่ามีความก้าวล้ำในบางประการ - การรวมค่าคงที่ของ Ryberg และค่าคงที่ของพลังค์ (ทฤษฎีควอนตัม) กับแบบจำลองของรัทเธอร์ฟอร์ด - มันได้รับความทุกข์ทรมานจากข้อบกพร่องบางอย่าง สำหรับผู้เริ่มต้นสันนิษฐานว่าอิเล็กตรอนมีทั้งรัศมีและวงโคจรที่รู้จักสิ่งที่เวอร์เนอร์ไฮเซนเบิร์กจะพิสูจน์หักล้างในอีกสิบปีต่อมาด้วยหลักการความไม่แน่นอนของเขา
นอกจากนี้แม้ว่ามันจะมีประโยชน์ในการทำนายพฤติกรรมของอิเล็กตรอนในอะตอมไฮโดรเจน แต่แบบจำลองของบอร์ก็ไม่ได้มีประโยชน์ในการทำนายสเปกตรัมของอะตอมที่มีขนาดใหญ่ขึ้น ในกรณีเหล่านี้ที่อะตอมมีอิเล็กตรอนหลายตัวระดับพลังงานไม่สอดคล้องกับที่คาดการณ์ไว้ในบอร์ โมเดลไม่ทำงานกับอะตอมฮีเลียมที่เป็นกลาง
แบบจำลอง Bohr นั้นไม่สามารถอธิบายปรากฏการณ์ Zeeman Effect ซึ่งเป็นปรากฏการณ์ที่นักฟิสิกส์ชาวดัตช์ได้กล่าวไว้ในปี 1902 โดยที่เส้นสเปกตรัมถูกแยกออกเป็นสองส่วนหรือมากกว่านั้นในสนามแม่เหล็กภายนอกที่คงที่ ด้วยเหตุนี้จึงมีการปรับแต่งหลายครั้งโดยใช้แบบจำลองอะตอมของ Bohr แต่สิ่งเหล่านี้พิสูจน์แล้วว่าเป็นปัญหา
ในท้ายที่สุดสิ่งนี้จะนำไปสู่รูปแบบของ Bohr ที่ถูกแทนที่ด้วยทฤษฎีควอนตัมซึ่งสอดคล้องกับงานของ Heisenberg และ Erwin Schrodinger อย่างไรก็ตามแบบจำลองของ Bohr ยังคงมีประโยชน์ในฐานะเครื่องมือการเรียนการสอนสำหรับการแนะนำนักเรียนให้รู้จักกับทฤษฎีสมัยใหม่มากขึ้นเช่นกลศาสตร์ควอนตัมและแบบจำลองอะตอมของวาเลนซ์เชลล์
มันจะพิสูจน์ให้เห็นว่าเป็นก้าวสำคัญในการพัฒนาแบบจำลองมาตรฐานของฟิสิกส์ของอนุภาคแบบจำลองที่โดดเด่นด้วย "เมฆอิเล็กตรอน" อนุภาคมูลฐานและความไม่แน่นอน
เราได้เขียนบทความที่น่าสนใจมากมายเกี่ยวกับทฤษฎีอะตอมที่นี่ที่นิตยสารอวกาศ แบบจำลองอะตอมของจอห์นดัลตันรูปแบบพลัมพุดดิ้งคืออะไรแบบจำลองอิเลคตรอนเมฆคืออะไรใครคือพรรคประชาธิปัตย์และใครคือส่วนของอะตอม
นักดาราศาสตร์ยังมีบางตอนในเรื่อง: ตอนที่ 138: กลศาสตร์ควอนตัม, ตอนที่ 139: ระดับพลังงานและ Spectra, ตอนที่ 378: รัทเธอร์ฟอร์ดและอะตอมและตอนที่ 392: โมเดลมาตรฐาน - อินโทร
แหล่งที่มา:
- Niels Bohr (1913)“ ตามรัฐธรรมนูญของอะตอมและโมเลกุลตอนที่ 1”
- Niels Bohr (1913)“ ตามรัฐธรรมนูญของอะตอมและโมเลกุลส่วนที่ II มีเพียงนิวเคลียสเดียว”
- สารานุกรมบริแทนนิกา: Borh Atomic Model
- Hyperphysics - Bohr Model
- มหาวิทยาลัยเทนเนสซีนอกซ์วิลล์ - รุ่น Borh
- มหาวิทยาลัยโตรอนโต - The Bohr Model of the Atom
- นาซา - จินตนาการถึงจักรวาล - ความเป็นมา: อะตอมและพลังงานแสง
- เกี่ยวกับการศึกษา - แบบจำลองของบอร์ของอะตอม