ในปลายศตวรรษที่ 19 นักเคมีชาวรัสเซีย Dmitri Mendeleev ตีพิมพ์ความพยายามครั้งแรกของเขาในการจัดกลุ่มองค์ประกอบทางเคมีตามน้ำหนักอะตอมของพวกเขา ในขณะนั้นมีองค์ประกอบประมาณ 60 รายการเท่านั้น แต่ Mendeleev ตระหนักว่าเมื่อองค์ประกอบถูกจัดเรียงตามน้ำหนักจะมีองค์ประกอบบางประเภทเกิดขึ้นในช่วงเวลาปกติหรือช่วงเวลา
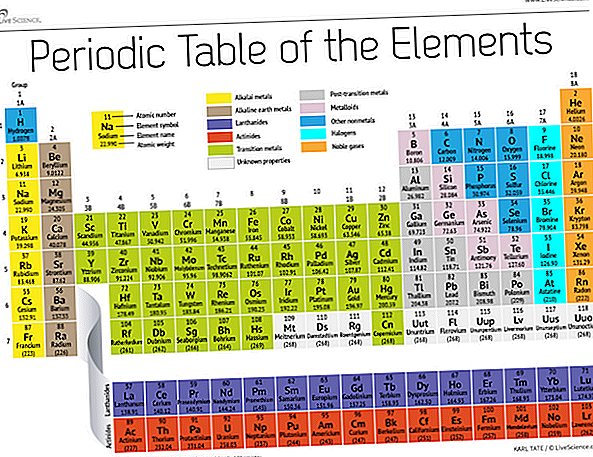
วันนี้ 150 ปีต่อมานักเคมีจำองค์ประกอบ 118 อย่างเป็นทางการ (หลังจากเพิ่มผู้มาใหม่สี่คนในปี 2559) และยังคงใช้ตารางธาตุของ Mendeleev เพื่อจัดระเบียบพวกมัน ตารางเริ่มต้นด้วยอะตอมไฮโดรเจนที่ง่ายที่สุดจากนั้นจัดองค์ประกอบที่เหลือตามหมายเลขอะตอมซึ่งก็คือจำนวนของโปรตอนแต่ละอันที่มี ด้วยข้อยกเว้นจำนวนหนึ่งคำสั่งขององค์ประกอบจะสอดคล้องกับมวลที่เพิ่มขึ้นของแต่ละอะตอม
ตารางมีเจ็ดแถวและ 18 คอลัมน์ แต่ละแถวแสดงถึงหนึ่งช่วงเวลา จำนวนช่วงเวลาขององค์ประกอบแสดงจำนวนระดับพลังงานของอิเล็กตรอนที่อยู่ในบ้าน ยกตัวอย่างเช่นโซเดียมอยู่ในช่วงที่สามซึ่งหมายความว่าโซเดียมอะตอมมักจะมีอิเล็กตรอนในระดับพลังงานสามระดับแรก การเลื่อนลงของตารางมีระยะเวลานานขึ้นเนื่องจากใช้อิเล็กตรอนมากขึ้นเพื่อเติมเต็มระดับนอกที่ใหญ่กว่าและซับซ้อนมากขึ้น
คอลัมน์ของตารางแสดงถึงกลุ่มหรือตระกูลขององค์ประกอบต่างๆ องค์ประกอบในกลุ่มมักจะมีลักษณะและการทำงานที่คล้ายกันเพราะพวกเขามีอิเล็กตรอนจำนวนเท่ากันในชั้นนอกสุด - ใบหน้าที่พวกเขาแสดงให้โลกเห็น องค์ประกอบกลุ่มที่ 18 ที่ด้านขวาสุดของตารางมีเปลือกนอกเต็มสมบูรณ์และไม่ค่อยมีส่วนร่วมในปฏิกิริยาเคมี
โดยทั่วไปองค์ประกอบจะถูกจัดประเภทเป็นโลหะหรือไม่ใช่โลหะ แต่เส้นแบ่งระหว่างทั้งสองนั้นเป็นฝอย องค์ประกอบโลหะมักจะเป็นตัวนำไฟฟ้าและความร้อนที่ดี กลุ่มย่อยภายในโลหะขึ้นอยู่กับลักษณะที่คล้ายกันและคุณสมบัติทางเคมีของคอลเลกชันเหล่านี้ คำอธิบายของตารางธาตุของเราใช้การจัดกลุ่มองค์ประกอบที่เป็นที่ยอมรับกันทั่วไปตามห้องปฏิบัติการแห่งชาติลอสอาลามอส
โลหะอัลคาไล: โลหะอัลคาไลทำขึ้นส่วนใหญ่ของกลุ่ม 1 ซึ่งเป็นคอลัมน์แรกของตาราง เงางามและอ่อนนุ่มพอที่จะตัดด้วยมีดโลหะเหล่านี้เริ่มต้นด้วยลิเธียม (Li) และจบด้วยแฟรนเซียม (Fr) พวกมันยังมีปฏิกิริยามากและจะระเบิดเป็นเปลวไฟหรือระเบิดเมื่อสัมผัสกับน้ำดังนั้นนักเคมีจึงเก็บไว้ในน้ำมันหรือก๊าซเฉื่อย ไฮโดรเจนที่มีอิเลคตรอนตัวเดียวก็อาศัยอยู่ในกลุ่มที่ 1 ด้วยเช่นกัน
โลหะอัลคาไลน์เอิร์ ธ : โลหะอัลคาไลน์เอิร์ ธ ทำขึ้นกลุ่ม 2 ของตารางธาตุจากเบริลเลียม (Be) ถึงเรเดียม (Ra) แต่ละองค์ประกอบเหล่านี้มีอิเล็กตรอนสองตัวที่อยู่ในระดับพลังงานสูงสุดซึ่งทำให้ดินอัลคาไลน์มีปฏิกิริยาพอที่จะพบได้เพียงลำพังในธรรมชาติ แต่พวกมันไม่ได้มีปฏิกิริยาเหมือนโลหะอัลคาไล ปฏิกิริยาทางเคมีของพวกเขามักจะเกิดขึ้นช้ากว่าและผลิตความร้อนน้อยกว่าเมื่อเทียบกับโลหะอัลคาไล
lanthanides: กลุ่มที่สามยาวเกินไปที่จะใส่ลงในคอลัมน์ที่สามได้ดังนั้นมันจึงแตกออกและพลิกด้านข้างเพื่อกลายเป็นแถวบนสุดของเกาะที่ลอยอยู่ที่ด้านล่างของตาราง นี่คือแลนทาไนด์, องค์ประกอบ 57 ถึง 71 - แลนทานัม (La) ถึงลูเทเนียม (Lu) องค์ประกอบในกลุ่มนี้มีสีขาวเงินและทำให้เสื่อมเสียเมื่อสัมผัสกับอากาศ
actinides: แอคติไนด์จะเรียงแถวด้านล่างของเกาะและประกอบด้วยองค์ประกอบ 89, แอคติเนียม (Ac), ผ่าน 103, ลอเรนเซียม (Lr) องค์ประกอบเหล่านี้มีเพียงทอเรียม (Th) และยูเรเนียม (U) เท่านั้นที่เกิดขึ้นตามธรรมชาติบนโลกในปริมาณที่มาก ทั้งหมดมีกัมมันตภาพรังสี แอคติไนด์และแลนทาไนด์รวมกันเป็นกลุ่มที่เรียกว่าโลหะทรานซิชันชั้นใน
โลหะทรานซิชัน: กลับไปที่เนื้อหาหลักของตารางส่วนที่เหลือของกลุ่มที่ 3 ถึง 12 เป็นตัวแทนของโลหะทรานซิชันที่เหลือ องค์ประกอบเหล่านี้เป็นสิ่งที่คุณมักนึกถึงเมื่อคุณได้ยินคำว่าโลหะแข็ง แต่อ่อนนุ่มเป็นประกายและมีการนำไฟฟ้าที่ดี เพลงฮิตที่ยิ่งใหญ่ที่สุดในโลกหลายแห่งรวมถึงทองคำเงินเหล็กและทองคำขาวอาศัยอยู่ที่นี่
โลหะหลังการเปลี่ยนแปลง: ก่อนที่จะก้าวเข้าสู่โลกที่ไม่ใช่โลหะคุณลักษณะที่ใช้ร่วมกันจะไม่ถูกแบ่งอย่างเป็นระเบียบตามแนวตั้งของกลุ่ม โลหะหลังการเปลี่ยนแปลงคืออลูมิเนียม (Al), แกลเลียม (Ga), อินเดียม (ใน), แทลเลียม (Tl), ดีบุก (Sn), ตะกั่ว (Pb) และบิสมัท (Bi) และพวกมันครอบคลุมกลุ่ม 13 ถึงกลุ่ม 17 องค์ประกอบเหล่านี้มีลักษณะคลาสสิกบางส่วนของโลหะทรานซิชัน แต่ก็มีแนวโน้มที่จะนิ่มกว่าและมีคุณภาพต่ำกว่าโลหะทรานซิชันอื่น ๆ ตารางธาตุหลายแห่งจะมีเส้น "บันได" ที่เป็นตัวหนาด้านล่างของโบรอนที่เชื่อมต่อในแนวทแยงกับแอสตาไทน์ คลัสเตอร์โลหะหลังการเปลี่ยนแปลงทางด้านซ้ายล่างของบรรทัดนี้
Metalloids: metalloids คือโบรอน (B), ซิลิกอน (Si), เจอร์เมเนียม (Ge), สารหนู (As), พลวง (Sb), เทลเลียม (เทล) และพอโลเนียม (Po) พวกเขาสร้างบันไดที่แสดงถึงการเปลี่ยนแปลงอย่างค่อยเป็นค่อยไปจากโลหะเป็นอโลหะ องค์ประกอบเหล่านี้บางครั้งทำงานเป็นสารกึ่งตัวนำ (B, Si, Ge) แทนที่จะเป็นตัวนำ Metalloids เรียกอีกอย่างว่า "semimetals" หรือ "metal poor"
อโลหะ: ทุกอย่างอื่นที่ด้านบนขวาของบันได - รวมทั้งไฮโดรเจน (H) ทางที่ติดค้างอยู่ในกลุ่มที่ 1 - ไม่ใช่อโลหะ เหล่านี้รวมถึงคาร์บอน (C), ไนโตรเจน (N), ฟอสฟอรัส (P), ออกซิเจน (O), กำมะถัน (S) และซีลีเนียม (Se)
ฮาโลเจน: องค์ประกอบสี่อันดับแรกของกลุ่ม 17 จากฟลูออรีน (F) ถึงแอสตาติน (At) แสดงถึงหนึ่งในสองส่วนย่อยของ nonmetals ฮาโลเจนนั้นมีปฏิกิริยาทางเคมีค่อนข้างมากและมีแนวโน้มที่จะจับคู่กับโลหะอัลคาไลเพื่อผลิตเกลือชนิดต่าง ๆ ยกตัวอย่างเช่นเกลือแกงในครัวของคุณคือการแต่งงานระหว่างโซเดียมโลหะอัลคาไลและคลอรีนฮาโลเจน
ก๊าซมีตระกูล: ไม่มีสีไม่มีกลิ่นและแทบไม่มีปฏิกิริยาใด ๆ เลยก๊าซเฉื่อยหรือก๊าซเฉื่อยก็ล้อมรอบโต๊ะในกลุ่มที่ 18 นักเคมีหลายคนคาดหวังว่า oganesson ซึ่งเป็นหนึ่งในสี่องค์ประกอบที่ได้รับการตั้งชื่อใหม่เพื่อแบ่งปันคุณสมบัติเหล่านี้ อย่างไรก็ตามเนื่องจากองค์ประกอบนี้มีการวัดครึ่งชีวิตในหน่วยมิลลิวินาทีจึงไม่มีใครสามารถทดสอบได้โดยตรง Oganesson เสร็จสิ้นช่วงเวลาที่เจ็ดของตารางธาตุดังนั้นหากใครก็ตามสามารถสังเคราะห์องค์ประกอบ 119 (และการแข่งขันที่จะทำเช่นนั้นกำลังดำเนินการอยู่) มันจะวนไปรอบ ๆ เพื่อเริ่มแถวที่แปดในคอลัมน์โลหะอัลคาไล
เนื่องจากธรรมชาติของวัฏจักรที่สร้างขึ้นตามช่วงเวลาที่ทำให้ชื่อของตารางนักเคมีบางคนชอบที่จะมองเห็นตารางของ Mendeleev เป็นวงกลม
เพิ่มเติม ทรัพยากร: